Mind ez idáig nem érkezett hivatalos kérelem a koronavírus elleni Szputnyik V orosz oltóanyag (Gam-COVID-Vak) fejlesztőitől sem a fokozatos szakvizsgálat (rolling review), sem pedig a forgalomba hozatali engedély folyamatának megkezdéséhez – közölte az Európai Gyógyszerügynökség (EMA) szerdán. A hágai székhelyű uniós ügynökség közleménye szerint a többfelé megjelent állítások ellenére az orosz vakcina fejlesztője nem nyújtott be kérelmet a koronavírus ellen kifejlesztett oltóanyagának uniós forgalomba hozatalára. Az EU gyógyszerfelügyeleti hatóságának szerepét betöltő ügynökség arról tájékoztatott, hogy
Még nem kérvényezték a Szputnyik V uniós engedélyeztetését
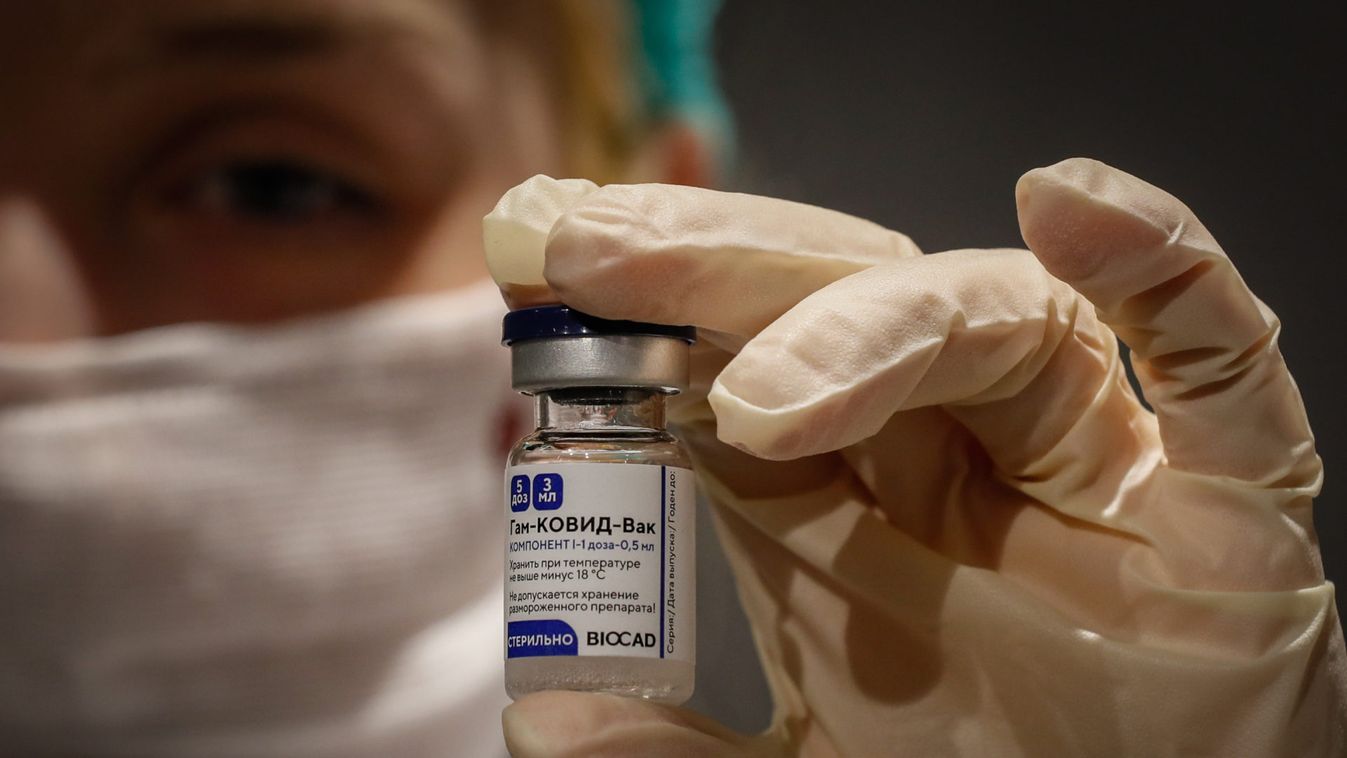
Az Európai Gyógyszerügynökség tagadta, hogy az oroszok már beadták volna a dokumentumokat.
a fejlesztők ez idáig tudományos tanácsokat kaptak az EMA-tól, biztosítva számukra a legújabb szabályozási és tudományos útmutatásokat az oltóanyagok kifejlesztéséhez.
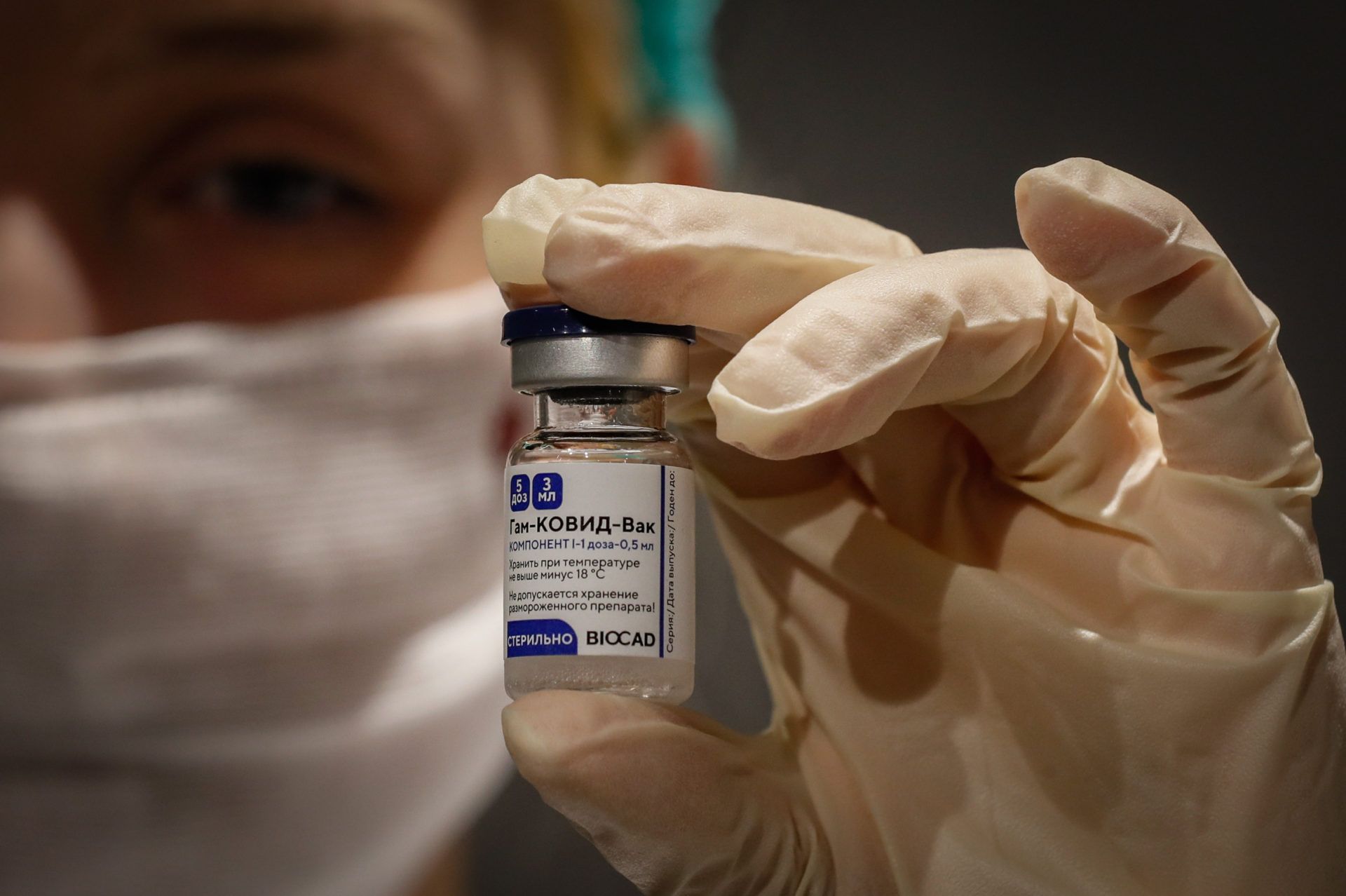
Fotó: MTI/EPA/Jurij Kocsetkov
Közölték az is, hogy az orosz fejlesztők kifejezték a koronavírus elleni oltóanyaguk folyamatos felülvizsgálati eljárásának megindítása iránt igényüket. AZ EMA kiemelte ugyanakkor, hogy a folyamatos felülvizsgálati eljárást csak a legígéretesebb gyógyszerek és oltások számára tartják fenn. Ahhoz, hogy a fejlesztők benyújthassák kérelmüket a folyamatos felülvizsgálati eljárás megindítására, az EMA humángyógyszer bizottsága (CHMP), valamint a koronavírus-világjárvánnyal foglalkozó munkacsoport (Covid–ETF) beleegyezése szükséges.
Leszögezték: az EMA mindig közzéteszi, amikor az ügynökséghez a fejlesztők részéről folyamatos felülvizsgálat iráni kérelem érkezik, és megkezdődik az értékelés. Hasonlóképpen közzéteszi azt is, ha az ügynökség hivatalos forgalomba hozatali kérelmet kap – tették hozzá.
Az orosz oltóanyagok fejlesztését finanszírozó Oroszországi Közvetlen Befektetési Alap (RFPI) kedden közölte, hogy benyújtotta a Covid–19 betegség elleni Szputnyik V vakcina bejegyzésére vonatkozó kérelmet az Európai Gyógyszerügynökséghez (EMA). Az RFPI 2021. január 29-én kérelmezte a Szputnyik V vakcina bejegyzését az Európai Unióban, és kezdeményezte az információátadást az EMA-nak a fokozatos szakvizsgálat (rolling review) eljárásán keresztül – áll az orosz alap közleményében.
Az Európai Bizottság korábban azt közölte, hogy az Európai Gyógyszerügynökség előzetes tárgyalásokat folytat a koronavírus elleni orosz vakcina, a Szputnyik V gyártójával, az orosz vállalat azonban még nem döntött úgy, hogy kérelmet nyújt be a készítmény uniós alkalmazásának jóváhagyására.
A téma legfrissebb hírei
Tovább az összes cikkhez
„A nemzeti gondolat és a magyar dollárbaloldal nem talál egymásra”
Deutsch Tamás szerint az Európai Parlamentben a saját hazád ellenében kiállni esküszegő magatartás.

Beteljesült Zelenszkij álma: titokban nagy hatótávolságú rakétákat kapott Amerikától
Kijev már be is vetette az ATACMS rakétákat, amelyekért sokáig könyörgött Washingtonnak.

Szijjártó Péter újabb kínai beruházást jelentett be
A kínai vállalatok a legmodernebb és legszofisztikáltabb technológiai megoldásokat igénylő ágazatokban is a világpiac vezetői közé tartoznak.

Ukrajna eltalált két oroszországi olajtárolót + videó
Négy frontszakaszról számolt be előretörésről az orosz védelmi minisztérium.
Ne maradjon le a Magyar Nemzet legjobb írásairól, olvassa őket minden nap!
- Iratkozzon fel hírlevelünkre
- Csatlakozzon hozzánk Facebookon és Twitteren
- Kövesse csatornáinkat Instagrammon, Videán, YouTube-on és RSS-en

Felbukkant egy újabb halálos vírus

Kiestek a mélyen kivágott felsőből Vajna Tímea hatalmas mellei

Megint lecsapott a Nyerő Páros átka, szakított a magyar műsorvezető és menyasszonya

Kiderült, hogy van 24 ezer magyar nyugdíjas, aki legalább 600 ezer forintot kap havonta

Nagyot fog zuhanni az üzemanyag ára, ekkor várható

Kiderült, ki a szerzője Magyar Péterék adatkezelési tájékoztatójának + videó

Alig takarja a melltartó az egykori szépségkirálynő mellét

Szexuális erőszak miatt letartóztattak két Premier League-focistát

Ronnie O’Sullivan kínos helyzetbe hozta az ellenfelét a sznúker-vb-n

A magyar játékos belépője pirosat ért a PL-ben, nagy meccsekről marad le + videó

A Liverpool elhasalt, Szoboszlai miatt pedig aggódhatunk

Hosszú idő után először ültek tárgyalóasztalhoz az oroszok és ukránok
Címoldalról ajánljuk
Tovább az összes cikkhez
„A nemzeti gondolat és a magyar dollárbaloldal nem talál egymásra”
Deutsch Tamás szerint az Európai Parlamentben a saját hazád ellenében kiállni esküszegő magatartás.

Beteljesült Zelenszkij álma: titokban nagy hatótávolságú rakétákat kapott Amerikától
Kijev már be is vetette az ATACMS rakétákat, amelyekért sokáig könyörgött Washingtonnak.

Szijjártó Péter újabb kínai beruházást jelentett be
A kínai vállalatok a legmodernebb és legszofisztikáltabb technológiai megoldásokat igénylő ágazatokban is a világpiac vezetői közé tartoznak.

Ukrajna eltalált két oroszországi olajtárolót + videó
Négy frontszakaszról számolt be előretörésről az orosz védelmi minisztérium.

















